水を知る5:水を構成する水素と酸素4
- 2012/02/11 16:24
- Category: 水の科学
前回の記事では、「電子の偏りを「極性」と呼び、水の性質を考える上で非常に重要なキーワードになります。」との言葉で締めました。酸素原子が電子を引っ張る力が強いために、水素原子が引っ張られ、電子の偏りが生じる「極性」。この極性によって生じる影響は、水分子の中だけにとどまりません。
いかなる状況に置いても1つの水分子が単独で成立することはあり得ません。目の前のコップに入っている水には、アボガドロ数程度の水分子がひしめき合っている状態です。つまり、1つの水分子が所有している「極性」は、他の水分子に影響を与えることになります。具体的に言うと、1つの水分子(Aとします)の水素原子が、別の水分子(Bとします)の酸素原子に近づく時、両者の間で弱い結合を引き起こすことになります。この結合を水素結合といいます。水分子内の水素原始と酸素原子をくっつけている共有結合のエネルギーが110kcal/molであるのに対し、AとBを結びつける水素結合は4.5kcal/molであり、共有結合と比べると圧倒的に弱いことが分かります。水分子は常に熱エネルギーによって動いているので、水素結合によって生じる結合は生じても、一瞬で離れます。それでも、水中のいたるところで「くっついたり・離れたり」が生じているため、瞬間的に近接している水分子がグループを組んでいるように水素結合で結びついていることがあります。これを水のクラスターと言います。クラスターは水の性質を考える上でとても重要なキーワードです。
画像/参考書籍:H2Oの生命科学―細胞生命のしくみ(著:中村 運)
参考書籍:水の書 (PNEモノグラフ)(著:荒田 洋治)
水分子の二つの水素原子、一つの酸素は「共有結合」という頑丈な結合によって成立しています。共有結合とは、互いの電子を共有することで生じる結合です。
この時、電子を引っ張る力の大きさは水素より酸素の方が大きい為、水素が酸素に引っ張られる形になります。よって、結合の形は図のように不均衡になります。この電子の偏りを「極性」と呼び、水の性質を考える上で非常に重要なキーワードになります。
画像/参考書籍:H2Oの生命科学―細胞生命のしくみ(著:中村 運)
水分子は水素原子2つと酸素原子1つが結合している分子です。ですが、水素と酸素はそれぞれ1種類だけではありません。というのは、それぞれの原子を構成する原子核に、質量の異なる同位体が存在するからです。
同位体
原子核は陽子と中性子によって構成されています。
原子番号=陽子の数
質量数=陽子の数+中性子の数
陽子、中性子、原子番号、質量数には上記の関係が成立しますが、原子番号が同じなのに、質量数が異なる元素が存在します。つまり、「中性子の数が違う」元素です。これを同位体と呼びます。
天然で存在する水素、酸素のの同位体は3種類です。ですが特殊な環境下においてのみ、水素は更に4種類、酸素は更に14種類の同位体が存在します。
同位体存在度(天然で存在するもののみ)
水素1(原子核に陽子が1個の元素。軽水素)
99.985%
水素2(原子核に陽子が1個/中性子が1個。重水素)
0.015%
水素3(原子核に陽子が1個/中性子が2個。三重水素)
微量
酸素16(原子核に陽子が8個/中性子が8個)
99.762%
酸素17(原子核に陽子が8個/中性子が9個)
0.038%
酸素18(原子核に陽子が8個/中性子が10個)
重い水と軽い水
何らかの方法により同位体を濃縮することで、様々な同位体の組み合わせを持った水が出来ます。水素は軽水素から重水素、三重水素になることで質量が2、3倍と跳ね上がります。したがって、通常の水と比べて物性が大きく異なります。
参考書籍:水の書 (PNEモノグラフ)(著:荒田 洋治)
GDVでは生体の測定だけでなく、水の測定も大きな内容として存在します。水は、私たちの生命にとって、生命活動を維持する上で欠かすことのできない大切なものでありながら、まだまだ分かっていない部分も多くあります。「水を知る」とのテーマで、水の世界の探究をしたいと思います。
◆◆◆
まず、何を水と表すのでしょうか。水は、「水素と酸素の化合物」であると定義することが出来ます。
水は水素と酸素の化合物である。化学式はH2Oで表される。
化学式を見れば分かりますが、水は二つの水素と一つの酸素が結合した物質です。
水素とは、原子番号1の元素で、あらゆる元素の中で最も軽い物質です。ビックバンにおいて最も最初に形成された原子で、宇宙に存在する原子のうち、91%を水素が占めるという豊富な原子です。
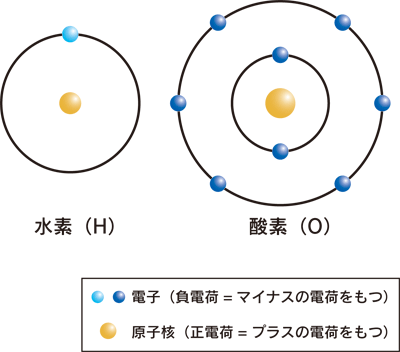
水素原子の構造は、中心に原子核があり、電子は1つだけ、核の周辺に存在します。
酸素とは、原子番号8の元素で、多くの元素と結合して化合物を作ります。宇宙における酸素原子の割合は全体の0.1%。水素に比べて著しく少ないですが、それでも全元素中第二位の存在率です(第三位の炭素は0.05%)。
酸素原子の構造は、水素原子よりも複雑です。中心にある原子核は、陽子8個・中性子8個で形成されています。その原子核の周囲に、合計8個の電子が存在しています。
画像
http://www.spring8.or.jp/ja/news_publications/research_highlights/no_54/ から
水素とは何か、酸素とは何かも、突き詰めて行けばとても深いテーマになりますので、今のところはここまでの定義で置いておくことにします。
つまり水は、宇宙の中で最も多く存在している2つの原子から成立している化合物であります。非常にありふれている存在ですが、その物性は極めて他の物質とは異なる性質を持っています。
次回から、水の定義を更に追いながら、少しずつ水についての理解を深めていきたいと思います。
参考書籍:H2Oの生命科学―細胞生命のしくみ(著:中村 運)
コップに入れた水は無色透明なのに対し、海や湖は青く見えたり、黒く見えたりすることもあります。

http://naturanon.exblog.jp/11457484/
コップの水

http://toshi7toshi7toshi5126.ti-da.net/e2848443.html
青い海

http://photozou.jp/photo/show/263824/25710022
黒い海
これらの色の違いが生じる原因は、太陽の光と発色の関係にあります。太陽の光をプリズムに通すと、赤や橙、黄色、緑、青など、様々な色に分けられます。これらの色が混ざり合い、重なり合って、太陽の光は無色になっています。
海や湖が青く見える大きな原因は、水分子が黄色や赤付近の光を吸収し、補色である青緑色の光が水中のゴミやプランクトンなどに散乱されて水面に出てくるからです。
ゴミやプランクトンの少ない海は、透明度が高いために反射して返ってくる光がほとんど無く、結果的に黒く見える海になります。
厚生省(現厚生労働省)では、1985年に「美味しい水研究会」を作り、専門家の意見を参考にしながら、日本の美味しい水の要件をまとめました。
蒸発残留物*30~200mg/L
硬度*10~100mg/L
遊離炭酸*3~30mg/L
過マンガン酸カリウム消費量(有機物量)*3mg/L以下
臭気*3以下(TON)
残留塩素*0.4mg/L以下
〔蒸発残留物〕
カルシウム、マグネシウム、シリカ、ナトリウム等のミネラルの含有量。
多すぎるとしつこく硬い味になり、少なすぎると淡白な味になる。
〔硬度〕
カルシウム、マグネシウムの含有量。まろやかな味になるかの指標になる。
〔遊離炭酸〕
水中の炭酸ガス。新鮮で爽やかな味を与えるが、多すぎるとビリビリした感覚になる。
〔過マンガン酸カリウム消費量(有機物量〕
水中の有機物(動物の排泄物・動植物の腐敗物質・肥料等)の量。
多いと水をまずく感じる。
〔臭気〕
水の臭い。排水や下水の混入等により生じる。
〔残留塩素〕
水中に残っている消毒用の塩素。
************
これは日本の基準であり、欧米や欧州では条件や基準が変わってきます。日本は自然の水がほぼ軟水なので、欧州特有の硬水を飲むと「まずい」と感じることが多くあります。
実験とは、「現象から推測される仮説をもとに検証を行う作業」です。その仮説が真実であるか証明するには、「一定条件で同一の現象を繰り返すことが出来る」こと、すなわち「再現性」が必要です。実験には水が用いられることが多く、水の純度によって実験結果に影響が左右されることも少なくありません。首尾よく実験するために、高い純度の実験用水を用いることが極めて重要になります。水の純度を高めるために、様々な精製法が存在します。
1. イオン交換法
〔定義〕イオン交換樹脂を用いる精製法
〔長所〕イオン除去に優れている・再生が可能
〔短所〕樹脂表面で微生物が繁殖する・再生に手間がかかる
2. 連続イオン交換(EDI)
〔定義〕電極・イオン交換膜・少量のイオン交換樹脂から構成されるEDIによる精製法
〔長所〕無機イオンの除去に優れている・イオン交換樹脂の再生が不要
〔短所〕樹脂の不純物付着を防ぐため、逆浸透膜による前処理が必要
3. 活性炭
〔定義〕活性炭(多孔性炭素質吸着剤)を用いた精製法
〔長所〕溶解有機物、塩素の除去に優れている
〔短所〕活性炭層内で微生物が繁殖する・吸着容量に限度がある
4. デプスフィルター
〔定義〕木綿やポリプロピレンなどの繊維を重ね合わせたフィルターによる精製法
〔長所〕目詰まりしにくく、汚れの保持力に優れる
〔短所〕圧力変動や流量変動により、粒子やフィルター素材が二次側に流出する
5. メンブランフィルター
〔定義〕窓の格子やふるいのような均一な構造をもつフィルターによる精製法
〔長所〕孔径より大きな分子(微粒子・微生物)を確実に捕捉する
〔短所〕目詰まりを起こしやすい
6. 限外ろ過膜(UF)
〔定義〕孔径100nm以下である限外ろ過膜を用いた精製法
〔長所〕エンドキシン、Rnase、コロイド状物質を除去できる
〔短所〕定期的に膜の洗浄が必要
7. 逆浸透膜(RO)
〔定義〕逆浸透膜というろ過膜を用いた精製法
〔長所〕無機物・有機物・微生物・微粒子を効果的に除去
〔短所〕精製された水の水質が原水の水質の影響を受ける
8. 脱気膜
〔定義〕脱気技術液体中から溶存ガスを取り除く技術
〔長所〕溶存ガスを除去する最も簡便な方法
〔短所〕真空ポンプや不活性ガスなどの機器が必要
9. 蒸留
〔定義〕物質の揮発性、沸点の違いを利用し、不純物を含む水から水を気化させて回収する精製法
〔長所〕水中の不純物を全般的に除去
〔短所〕精製速度が遅く、原水の飛沫同伴により水質が劣化
10. 紫外線(UV)
〔定義〕紫外線を照射することによる精製法
〔長所〕殺菌に有効で、有機物の酸化分解が出来る
〔短所〕後段でイオン交換樹脂などによる精製が必要
水の磁気処理により、様々な水の変化が齎されることはよく言われます。その中でも、興味深い物の一つとして、「接触角の低下」があります。
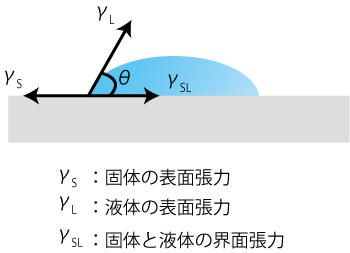
接触角とは、図のθの部分を指します。
2006年に学会誌「銅と銅合金(45巻1号 2006年)」に掲載された「りん脱酸銅の腐食への磁気処理水効果」という論文中には、水の磁気処理による効果について以下の記述があります。
磁気処理によって接触角が低下した水の中では、Cu^2+の溶出が劇的に抑制されることが分かった。
これは換言すれば水の磁気処理により、銅の酸化が抑制される→銅の腐食を抑制することが出来るということになります。
この論文の中の実験を行った信州大学、神戸製鋼所の方は銅の腐食を防止できるかどうかまでは確認されておられませんが、可能性として非常に興味深い内容を示唆されておられます。
GDVによって水を計測する際、シリンジを用いて水を測定する手法がありますが、この場合は水の表面張力に大きく依存します。接触角の違いが齎すGDVパラメータの変化について、研究する余地は大いにあります。
*参考
新しい局面を迎えた界面の分子科学―機能デザインと計測技術の展開
編集 日本化学会りん脱酸銅の腐食への磁気処理水効果
(学会誌 銅と銅合金 45巻1号 2006年)